
预约高中1对1精品课程(面授/在线),满足学员个性化学习需求 马上报名↓
2019年初中化学复习知识点:原子。同学们在初三的时候先进次接触了化学这一学科,同学们学习的先进个化学知识点就是元素字母,比如说今天小编要为大家介绍的原子,同学们知道多少关于原子的知识呢,下面为大家带来2019年初中化学复习知识点:原子,希望对同学们提供帮助。
想要了解【初中化学】的相关资料,请点击加入【爱智康初中交流福利群】 ,并直接向管理员“小康康”索取!爱智康初中交流福利群会不定期免费发放学习资料,初中以及中考政策等相关消息,请持续关注!
,并直接向管理员“小康康”索取!爱智康初中交流福利群会不定期免费发放学习资料,初中以及中考政策等相关消息,请持续关注!
2019年初中化学复习知识点:原子
原子的构成
质子:1个质子带1个单位正电荷原子核(+)
中子:不带电原子不带电
电子:1个电子带1个单位负电荷
1.构成原子的粒子有三种:质子、中子、电子。但并不是所有的原子都是由这三种粒子构成的。如有一种氢原子中只有质子和电子,没有中子。
2.在原子中,原子核所带的正电荷数(核电荷数)就是质子所带的电荷数(中子不带电),而每个质子带1个单位正电荷,因此,核电荷数=质子数,由于原子核内质于数与核外电子数相等,所以在原子中核电荷数=质子数=核外电子数。
原子中存在带电的粒子,为什么整个原子不显电性?
原子是由居于原子中心带正电的原子核和核外带负电的电子构成,原子核又是由质子和中子构成,质子带正电,中子不带电;原子核所带正电荷(核电荷数)和核外电子所带负电荷相等,但电性相反,所以整个原子不显电性。
原子定义
原子:化学变化中的较小微粒。
(1)原子也是构成物质的一种微粒。例如少数非金属单质(金刚石、石墨等);金属单质(如铁、汞等);稀有气体等。
(2)原子也不断地运动着;原子虽很小但也有一定质量。对于原子的认识远在公元前5世纪提出了有关原子的观念。但没有科学实验作依据,直到19世纪初,化学家道尔顿根据实验事实和严格的逻辑推导,在1803年提出了科学的原子论。
原子核外电子的排布
1、原子中电子的运动是分开运动的,在含多电子的原子里,电子的能量不同能量低的,通常在离核近的区域运动。能量高的,通常在离核远的区域运动。
为了便于说明问题,通常就用电子层来表明运动着的电子离核远近的不同。把能量较低、离核较近的叫先进层,能量稍高、离核稍远的叫第二层,由里往外依次类推,叫三、四、五、六、七层(也可分别叫KLMNOPQ层)。电子的这种分开运动是没有固定轨道的。
2、原子结构示意图的认识
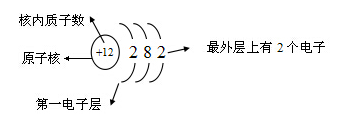
(1)1~20号元素,先进层较多能排2个,其它层较多能排8个,不足的,是几个就排几个。各层电子数之和等于质子数,原子较外层电子数决定了元素的化学性质!
(2)稀有气体元素较外层一般为8个(氦为2),为相对稳定的结构。
(3)非金属元素较外层一般多于4个,在化学反应中易得到电子,形成阴离子,从而达到相对稳定的结构。
(4)金属元素较外层一般少于4个,在化学反应中易失去电子,形成阳离子,从而达到相对稳定的结构。
小编推荐:
这一期的2019年初中化学复习知识点:原子小编就介绍到这里,希望对有需要的同学提供帮助,养成好的学习习惯:预习、笔记、复习、题目,归纳总结,甚至是草稿、解题步骤等,都需要用心去做。因此建议同学们在初中阶段尽可能养成好的学习习惯,为接下来学习做好准备、蓄力。更多试题辅导,请拨打免费咨询电话: !
!